A redoxireakció
A kémiai reakciókat több szempont alapján is csoportosíthatjuk!
- Részecskeszám-változás alapján létezik: egyesülés és bomlás
- Hőváltozás szempontjából létezik: endoterm reakció és exoterm reakció
- Részecskeátmenet alapján létezik: sav-bázis reakció és Redoxireakció
A redoxi szó két különböző szó rövidítéséből lett összetéve. A redukció és az oxidáció szó rövidítéséből.
Kiterjedt jelentésük:
- Redukciónak nevezzük az elektronfelvételt. Ez bármelyik elem vagy vegyület elektronfelvételét jelentheti, függetlenül attól, hogy a folyamatban jelen volt-e az oxigén.
- Oxidációnak nevezzük az elektronleadással járó folyamatokat, változásokat. Az, hogy egy elem elektront ad le, már ismerős az ionokkal kapcsolatos fejezetekből. Így keletkeznek a kationok.
Példa oxidációra:
Az alábbi reakcióban a nátrium elektront ad le a klórnak, tehát oxidálódik. Azok az elemek, vegyületek, amelyek könnyen adnak le elektront, vagyis könnyen oxidálódnak, jó redukálószerek.
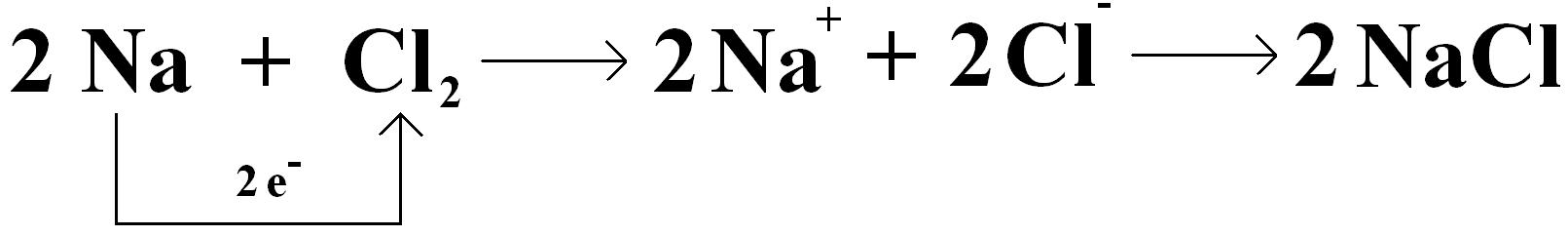 Ebben a reakcióban megvan a példa a redukcióra is:
Ebben a reakcióban megvan a példa a redukcióra is: Hiszen az az elem, amelyik felveszi az elektront, redukálódik. Tehát oxidálószer.Láthatjuk tehát, hogy a redukció és az oxidáció folyamata mindig egymás mellett játszódik le, ezért is hívják az elektronátadással járó folyamatokat redoxireakcióknak.
 | Tanulja meg a kémiát
az Ön gyermeke is játszva!
Rendelje meg a Kémiából Ötös
oktató DVD-t most !

|